Термодинамические и кинетические основы химического процесса
Задача 1-1. Используя термодинамические данные, рассчитать константу равновесия газофазной реакции гидратации этилена при температуре 300 С (573 К):
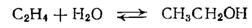
Скачать решение задачи 1-1 (цена 100р)
Задача 1-2. При исследовании реакции разложения аммиака на вольфраме
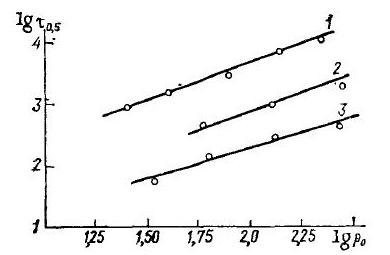
Рисунок 1.1 Значения температуры при 1 – 900; 2 - 1100
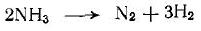
при различных температурах получены следующие зависимости времени полупревращения т0,5 от наального давления паров аммиака ро (продукты разложения при т = 0 отсутствуют): Определить порядок реакции и энергию активации.
Скачать решение задачи 1-2 (цена 100р)
Задача 1-3. При исследовании реакции взаимодействия трифенилметилхлорида с метанолом в безводном бензоле в присутствии пиридина при температуре 25°С, начальной концентрации трифенилметилхлорида 0,106 кмоль*м-3 и начальной концентрации метанола 0,054 кмоль*м-3 были получены следующие данные:
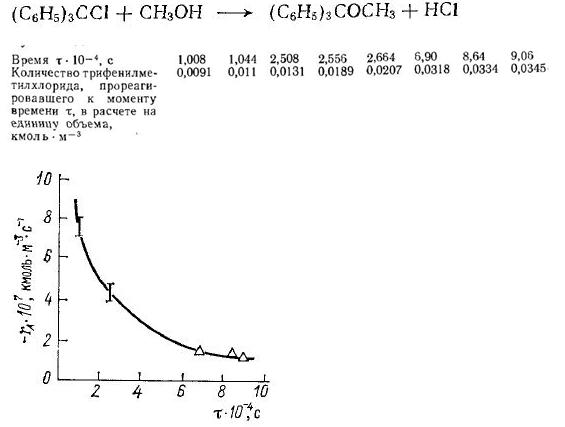
Определить константу скорости реакции и построить график зависимости скорости реакции от времени.
Скачать решение задачи 1-3 (цена 100р)
Задача 1-4. При проведении реакции изомеризации этилового эфира ацетилуксусной кислоты было экспериментально установлено, что мольная доля енолыюй формы изменяется со временем следующим образом и при равновесии равна 0,078. Определить k.
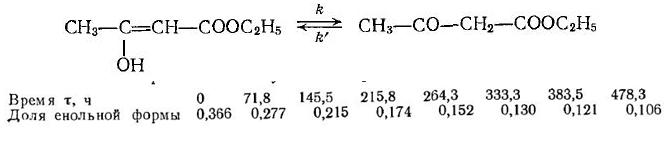
Скачать решение задачи 1-4 (цена 100р)
Задача 1-5. Реакция проводится в среде абсолютного этанола. Для опыта было взято 20 см3 0,1 н. раствора исходной кислоты. Полученные данные приведены ниже: Определить константы скорости реакции k1 и k2
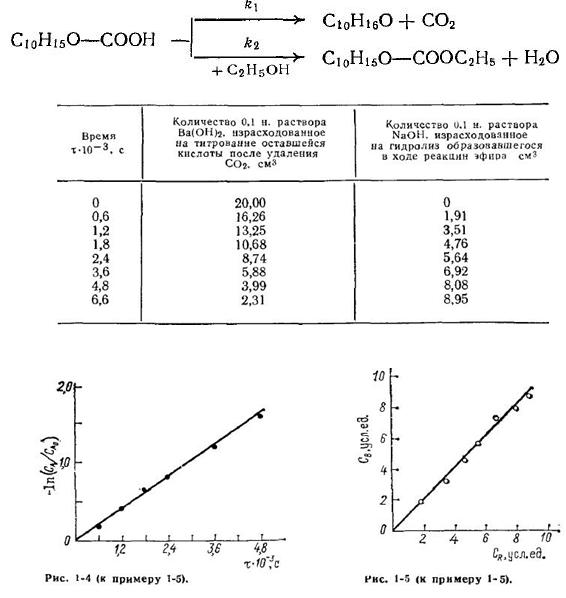
Скачать решение задачи 1-5 (цена 100р)
Задача 1-6. При проведении газофазной реакции разложения тетрагидрофурана Оыла получена следующая зависимость скорости реакции в начальный момент (dp/dт)макс от начального давления тетрагидрофурана р0: При различных температурах получены следующие значения т05 в зависимости от р0:
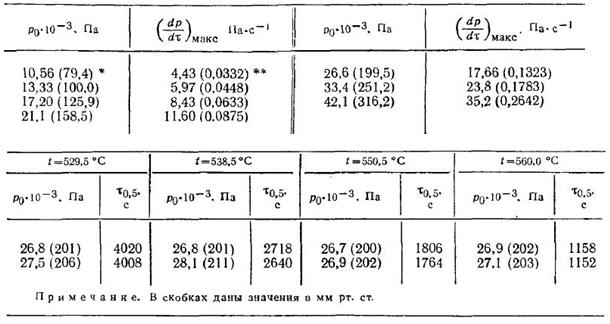
Определить порядок реакции и величину энергии активации.
Скачать решение задачи 1-6 (цена 100р)
Задача 1-7. Реакция окисления этилена кислородом воздуха в присутствии катализатора (серебра):
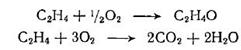
проходит в реакторе непрерывного действия при Т = 533 К и атмосфером давлении. Известно, что газовый поток, поступающий в реактор, содержит 5% (мол.) этилена и 95% (мол.) воздуха. При данных условиях 50% этилена окисляется до окиси этилена и 40% этилена сгорает. Рассчитать тепловой эффект реакции, отнесенный к 1 моль этилена.
Скачать решение задачи 1-7 (цена 100р)
