Задание 4 вар 1 Получение сульфида натрия |
|||||||||||||||||||||||
| 2 Производство сульфида натрия восстановлением сульфата Сульфат натрия размолотый до размера зерен 1-2 мм шнековым питателем подают во вращающуюся печь, где при 400-500 С происходит его взаимодействие с водородом, подаваемым противотоком. Полученный | |||||||||||||||||||||||
|
| |||||||||||||||||||||||
| ( ОХТ ) |
|||||||||||||||||||||||
|
pуб 400
|
|||||||||||||||||||||||
|
2 Производство сульфида натрия восстановлением сульфата 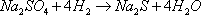
1. Составить и описать технологическую схему получения сульфида натрия восстановлением сульфата. 2. Составить материальный баланс процесса. 3. Рассчитать технологические и технико-экономические показатели. Файл помощи оформления заказа и порядок (инструкция) его получения Краткая теория процесса Восстановление сульфата натрия природным газом или метаном, вероятно, связано с диссоциацией последнего, происходящей при высоких температурах (800-1000°). Разложение метана ускоряется в присутствии древесного угля, кокса, железа, никеля и др. Выход Na2S При 600° незначительный, сильно возрастает выше 750°, при 800° за 3 ч достигает -88%, а при 850°-95%. Более высокая температура приводит к загрязнению продукта углеродом, выделяющимся при разложении метана, а более длительное нагревание -к образованию побочных продуктов. При восстановлении не выше 850° содержание углерода в продукте меньше 1 % 88<89. Na2SO4 + Н2 + ЗСО = Na2CO3 + H2S + 2СO2 Na2SO4 + 2Н2 + 2СО = Na2CO3 + H2S + СO2 + Н2O |
|||||||||||||||||||||||
|
|
|||||||||||||||||||||||
Поиск, обзор и навигация
Магазин работ
ПиАХТ
Чертежи



