Раздел 1 и 2. Основные показатели химического производства и закономерности химических процессов
Задача 1-1 Химический состав оконного (силикатного) стекла выражается формулой Na2O*CaO*6SiO2, т.е. оно состоит из соды Na2O, известняка CaO и песка SiO2. Рассчитать теоретические коэффициенты по сырью при производстве стекла, если сода содержит 93,8% Na2CO3, известняк – 90,5% CaCO3 и песок – 99,0% SiO2.
Скачать решение задачи 1-1 (В.И. Игнатенков, В.С Бесков) (цена 150р)
Задача 1-2. Сколько потребуется сульфата железа FeSO4*7H2O и хромого ангидрида CrO3 для получения 1 т железохромого катализатора конверсии окиси углерода, имеющего состав: 90% - Fe2O3 и 10% - Cr2O3?
Скачать решение задачи 1.2 (В.И. Игнатенков, В.С Бесков) (цена 150р)
Задача 1-3 Негашенная известь содержит 94%, 12% и 4,8% примесей. Получается она обжигом известняка, содержащего 89% в негашенной извести получается из-за наличия в ней карбонатов еоличество которых определяет степень обжига известняка. определить расходный коэффициент известняка на 1 т извести указанного состава и степень обжига известняка.
Скачать решение задачи 1.3 (В.И. Игнатенков, В.С Бесков) (цена 150р)
Задача 1-4 Рассчитать расход колчедана, содержащего 40% S на 1 т H2SO4, если потери S и сернистого ангидрида в производстве серной кислоты составляют 3%, а степень абсорбции - 99%.
Скачать решение задачи 1-4 (В.И. Игнатенков, В.С Бесков) (цена 150р)
Задача 1-5 Рассчитать зависимость содержания кислорода в газах обжига от концентрации SO2 при воздушном дутье:
в) для обжига сернистого цинка ZnS.
Скачать решение задачи 1.5 (В.И. Игнатенков, В.С Бесков) (цена 150р)
Задача 1-7 Рассчитать расход бензола и пропан-пропиленовой фракции газов крекинга [30% (об.) пропилена и 70% (об.) пропана] для производства 1 т фенола, если выход изопропилбензола из бензола составляет 90% от теоретического, а фенола из изопропилбензола - 93%.
Молекулярная масса: бензола - 78, пропилена - 42, пропана - 44, фенола - 94.
Скачать решение задачи 1.7 (В.И. Игнатенков, В.С Бесков) (цена 150р)
Задача 1-8. Рассчитать расходные коэффициенты в производстве технического карбида кальция CaO + 3C = CaC2 + CO. Технический карбид кальция имеет следующий состав: 78 % СаС2, 15 % СаО, 3 % С, прочие примеси – 4 %. Известь содержит 96,5 % СаО. В коксе содержится 4% золы, 4 % летучих, 3% влаги. Молекулярные массы СаС2 – 64, СаО – 56.
Скачать решение задачи 1.8 (В.И. Игнатенков, В.С Бесков) (цена 150р)
Задача 1-9. Рассчитать основные технологические показатели производства бензола методом парофазовой дегидрогенизации циклогексана:
• теоретические и фактические расходные коэффициенты;
• выходы продуктов на подаваемый и превращенный циклогексан;
• общую и избирательную конверсии циклогексана.
Химическая схема процесса
C6H12 = C6H6 + 3H2
C6H12 = CH3C5H9
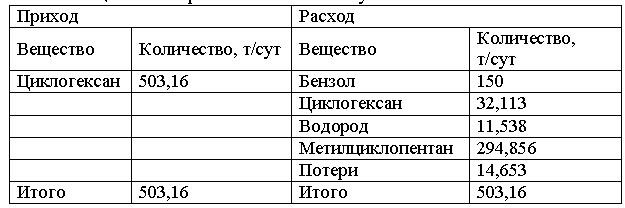
Материальный баланс производства метилциклопентана сведен в таблицу 1.
Таблица 1 – Материальный баланс получения бензола
Скачать решение задачи 1.9 (В.И. Игнатенков, В.С Бесков) (цена 150р)
Задача 1-11 Рассчитать расходные коэффициенты по сырью в производстве 1 т фосфата аммония (NH4)3PO4. Фосфорная кислота имеет концентрацию 58%, а аммиак содержит 2% влаги.
Скачать решение задачи 1.11 (В.И. Игнатенков, В.С Бесков) (цена 150р)
Задача 1-12 Рассчитать теоретический и практический коэффициенты 97% изопентана в производстве 1 т изопрена. Процесс каталитического дегидрирования изопентана осуществляется по реакциям:
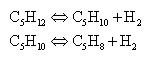
Выход изоамилена составляет 73%, а изопрена – 65% от теоретического.
Скачать решение задачи 1-12 (В.И. Игнатенков, В.С Бесков) (цена 150р)
Задача 2.1-1 Аккумуляторную кислоту (концентрация H2SO4 92,5%).нужно разбавить водой до содержания в ней 38% H2SO4. Сколько нужно взять воды для получения 180 кг разбавленной кислоты?
Скачать решение задачи 2.1-4 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-2 Сколько нужно взять купоросного масла (H2SO4 96%) и серной кислоты с концентрацией (H2SO4 64%), чтобы получить 2800кг 83%-ной H2SO4?
Скачать решение задачи 2.1-2 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-3 Сколько нужно взять растворов поваренной соли с концентрацией 310 и 230 г/л, чтобы получить 250 л раствора с концентрацией 280 г/л3
Скачать решение задачи 2.1-3 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-4 Азотную кислоту концентрацией 58% нужно разбавить водой до концентрации 46%. Сколько нужно взять воды, чтобы получить 2000кг разбавленной кислоты?
Скачать решение задачи 2.1-4 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-5. Влажность 150кг каменного угля при хранении на складе изменилась: а) с 8,4 до 3,9%; б) с 0,2 до 4%. Как изменилась масса угля?
Скачать решение задачи 2.1-5 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-6 Влажность 200кг серного колчедана при хранении на воздухе изменилась с 3 до 6% массовых долей. Как при этом изменилась масса колчедана?
Скачать решение задачи 2.1-6 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-7 Влажность 300кг извести при хранении изменилась с 2 до 5% массовых долей. Как при этом изменилась масса извести?
Скачать решение задачи 2.1-7 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-8. Определить расход бурого угля (70% массовых долей С), водяного пара и воздуха для получения 1000м генераторного газа, содержащего в объемных долях,%: СО-40, Н2 - 18, N2 - 42. Процесс газификации твердого топлива содержит две основные реакции:
C + H2O = CO + H2
2C + O2 = 2 CO
Скачать решение задачи 2.1-8 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-9 Определить расходные коэффициенты в производстве карбида кальция (технического), содержащего [% (масс.)]: CaC2 -85; CaO -5; C-3; прочие примеси- ост. Известь содержит 96,5% CaO. Содержание (%масс) в коксе: золы- 4, летучих - 4, влаги- 3.
Расчёт вести на 1 т технического продукта. Молекулярная масса: CaC2- 64, CaO- 56.
Скачать решение задачи 2.1-9 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-10 Рассчитать расходные коэффициенты при производстве 1 т фосфора разложением фосфоритного концентрата. Процесс описывается уравнением:
Ca3(PO4)2 + 5С + SiO2 = 3CaO*SiO2+2P+5CO
Концентрат содержит 25% массовых долей Р2О5, кокс - 94,5% массовых долей углерода, степень восстановления фосфора равна 0,85.
Скачать решение задачи 2.1-10 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-12 Рассчитать состав шихты в производстве глинозема из боксита, соды и известняка методом спекания. Исходный боксит содержит, массовые доли, %: Al2O3 - 50; SiO2 - 10; Fe2O3 - 20. Мольное отношение компонентов (модуль) в спеке: M1 = Na2O/(SiO2 + Fe2O3) = 1; M2 = CaO/SiO2 = 2. Известняк содержит 90 % массовых долей СаСО3, техническая сода - 96 % массовых долей Na2СO3. Расчет вести на 1000 кг боксита.
Скачать решение задачи 2.1-12 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-13 Определить расходный коэффициент по техническому карбиду кальция в производстве ацетилена. В техническом продукте содержится 83% CaC2, а степень превращения CaC2 в производстве равна 0,88.
CaC2 + 2H2 = Ca(OH)2 + C2H2
Скачать решение задачи 2.1-13 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-14. Определить расход бурого угля (70% масс. долей углерода), водяного пара и воздуха для получения 1000м генераторного газа, в состав которого входят %об: СО - 40, H2 - 18, N2 - 42.
Процесс газификации протекает по реакциям:
C + H2O = CO + H2
2C + O2 = 2CO
Скачать решение задачи 2.1-14 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-15 Составить материальный баланс процесса газификации 1 т кокса, идущей по реакциям
C + H2O = CO + H2 - 131 кДж
CO + H2O = CO2 + H2 + 42 кДж
В коксе содержится 3% массовых долей зольных примесей, массовое соотношение пар/кокс составляет 1,5, степень превращения углерода в коксе – 0,98, выход монооксида углерода – 0,90. Найти также общее количество подведенной теплоты.
Скачать решение задачи 2.1-15 (В.И. Игнатенков, В.С Бесков) (цена 150р)
Задача 2.1-16 Составить материальный баланс и рассчитать выход SO2 при обжиге 1000кг руды, содержащей 22% массовых долей серы в виде сульфида цинка (остальное –несгораемые примеси) и при подаче полуторакратного избытка воздуха по отношению к стехиометрии. Реакция обжига
2ZnS+3O2=2ZnO+2SO2
В огарке содержится 0,5% массовых долей серы.
Скачать решение задачи 2.1-16 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-17. При обжиге известняка образуется твердый продукт следующего состава:
CaO CO2 Балласт
Вариант 1 92 2,4 остальное
Вариант 2 94 1,2 остальное
В исходном сырье содердится CaCO3 масовые доли, %:
вариант 1 - 91;
вариант 2 - 89.
Определить расход известняка на 1 т целевого продукта в виде CaO и степень превращения CaCO3.
Скачать решение задачи 2.1-17 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-18 Обжиговый газ, состоящий из 8% объемных долей SО2 и 12% объемных долей О2, остальное азот, подвергнут окислению на катализаторе. Степень окисления SО2 - 88%. Рассчитать состав газа после окисления в процентах.
Скачать решение задачи 2.1-18 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-19 Воздух, подводимый к доменной печи, содержит, объёмные доли, %: O2 – 21,1; N2 – 77,3; водяных паров – 1,6. Сколько потребуется добавить к воздуху кислорода, чтобы его концентрация стала равной 25% объёмных долей?
Скачать решение задачи 2.1-19 (В.И. Игнатенков, В.С Бесков) (цена 150р)
Задача 2.1–21 Рассчитать конечный состав газовой смеси, если ее исходный состав в массовых долях, % (объемных долях, %): СН4 – 16,5 (20,7); С2Н6 – 9,7 (22,9); О2 – 44,9 (18,6); N2 – 28,9(37,8). Количество смеси – 1000 кг (1000 м3). Какой конечный состав смеси в объемных долях, % (массовых долях, %), если удалено: СН4 – 105 кг (150 м3); О2 – 300 м3 (150 кг); добавлено водяного пара – 200 м3 (100 кг)?
Скачать решение задачи 2.1-21 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-22. Определить соотношение между H2 и N2 в азотоводородной смеси на входе в реактор синтеза аммиака,если в газе на выходе из него содержится, объемные доли,%: NH3 - 17; N2 - 11; H2 - 72.
Скачать решение задачи 2.1-22 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-23 Определить производительность колонны синтеза аммиака объемом 4м, если нагрузка по газу на единицу объема реактора составляет 3000м/ч. равновесная степень превращения реагентов, взятых в стехиометрическом соотношении, составляет 0,26, а выход аммиака - 0,78.
Скачать решение задачи 2.1-23 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-24 В реакторе протекают реакции:
А+2В=R
R +В= S
А +В= 2Т
Начальные концентрации, кмоль/м3: СА0=2, СВ0=2,3, СR0=СS0=СТ0 =0. Объёмный расход реакционной смеси 5*10-2 м3/с; Выходные концентрации, кмоль/м3: СА=1,4, СR=0,2, СS=0,4.
Определить степени превращения вещества В по реакциям; производительность по продукту R.
Скачать решение задачи 2.1-24 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-25 В реакторе протекают жидко-фазные реакции:
А+В=R
А+А= S
2 S +В= Т+2D
R+А=Т
Определить производительность реактора по веществам R и S при следующих условиях:
СА0=2, СВ0=1,7, СА=0,1, СВ=0,5, СТ=0,15, СD=0,05 кмоль/м3; объёмный расход реакционной смеси 1*10-2 м3/с; СR0=СS0=СТ0=СD0=0.
Скачать решение задачи 2.1-25 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-26 В реакторе идеального смешения протекают реакции:
А+2В=R
R + В = S
3В= 2Т
2А+ В = S+В
Концентрация, кмоль/м3 СR0=СS0=СТ0=СD0=0, СА0=1, СR=0,05, СА=0,44, СS=0,33, СТ=0,14; Скорость подачи исходных веществ 5•10-3 м3/ч;. Определить производительность по исходному веществу В и по продукту D.
Скачать решение задачи 2.1-26 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-27 В реакторе в адиабатических условиях протекают реакции:
А+В=R+D
2B=P
2R=S
Начальные концентрации, кмоль/м3: СА0=0,1, СВ0=0,3, СR0=СD0=СP0=СS0=0. Выходные концентрации, кмоль/м3: СP=0,028, СS=0,012, СD=0,034. Тепловые эффекты реакций, кДж/кмоль: Qp1=1,1•105, Qp2=8,8•104, Qp3=4,7*104. Плотность реакционной смеси 860 кг/м3, её удельная теплоёмкость 2,85*10^3 Дж/(кг•град). Объёмный расход смеси 2,6*10-2 м3/с.
Определить производительность реактора по продукту R и температуру на выходе реактора, если начальная температура 12 С.
Скачать решение задачи 2.1-27 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-28 В реакторе в адиабатических условиях протекают реакции:
2А+В=R
R 2B= S
3В=2Т
Начальные концентрации, кмоль/м3: СА0=0,3, СВ0=0,2, СR0=СТ0= =СS0=0. Выходные концентрации, кмоль/м3: СВ=0,016, СS=0,011, СТ=0,03. Тепловые эффекты реакций, кДж/кмоль: Qp1=1,2•105, Qp2=6,8•104, Qp3=4,7•104. Плотность реакционной смеси 850 кг/м3, её удельная теплоёмкость 2,4•103 Дж/(кг•град). Объёмный расход смеси 3,4•10-2 м3/с.
Определить производительность реактора по продукту R и температуру на выходе реактора, если температура на входе 298 С.
Скачать решение задачи 2.1-28 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-29 Взаимодействие ацетилена с формальдегидом дает промежуточный –пропаргиловый спирт, а затем бутиндиол-1,4 по схеме
С2Н2 +СН2О => С3Н4О + СН2О => С4Н4О2
Степень превращения по ацетилену составляет 0,98, селективность по пропаргиловому спирту –0,66. Рассчитать необходимое количество ацетилена и формальдегида для получения 350 кг пропаргилового спирта в час.
Скачать решение задачи 2.1-29 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-30. Протекает обратимая реакция A + 2B = 2R + S. Начальные количества веществ, NA0 = 10, NB0 = 25, NR0 = 12 кмоль. В равновесной смеси NA = 2,5 кмоль.
Скачать решение задачи 2.1-30 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-31. Для реакции А+2В=2R, протекающей в жидкой фазе, определить степень превращения и соста реакционной смеси (CA, CB, CR) при xA = 0,45: 1) CA0 = 1; CB0 = 2; 2) CAO = 1, CBO = 1 кмоль/м3.
Скачать решение задачи 2.1-31 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-32 Определить состав реакционной смеси в конце процесса для реакции A + 3B = 2R, протекающей в жидкой фазе, если: 1) хА = 0,2; 2) хВ = 0,2; 3) СВ0 - 5 кмоль/м3.
Скачать решение задачи 2.1-32 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-33 Протекает реакция А=3R. Определить состав реакционной смеси на выходе из реактора, если САО = 1 кмоль/м3, хА = 0,5. Принять, что объем реакционной смеси не меняется.
Скачать решение задачи 2.1-33 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-34 В газовой фазе протекает реакция А+В=3R. Определить состав реакционной смеси в молярных долях, если
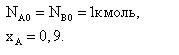
Скачать решение задачи 2.1-34 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-37 Для проведения реакции дегидратации этилового спирта
2С2Н5ОН = (С2Н5)2О + Н2О
взято исходное количество спирта, равное 24 моль, получено 8 моль эфира. Рассчитать состав полученной реакционной смеси, степень превращения реагента и выход продукта.
Скачать решение задачи 2.1-37 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-38 Для проведения реакции дегидратации этилового спирта
2С2Н5ОН = (С2Н5)2О + Н2О
взято исходное количество спирта, равное 24 моль, получено 8 моль эфира. Рассчитать состав полученной реакционной смеси, степень превращения реагента и выход продукта.
Скачать решение задачи 2.1-38 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-39 Протекают две параллельные реакции 2А=R и А=3S. Определить выход продукта R, степень превращения реагента А и селективность по продукту R, если на выходе из реактора известны количества веществ Na = 2моль, NR =NS = 3моль.
Скачать решение задачи 2.1-39 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-40 Протекают последовательные реакции А=2R и R=S. Определить степень превращения реагента А, выход и селективность по продукту R, если известен конечный состав реакционной смеси, кмоль/м3: CA = 1; CR = 2; CS = 2.
Скачать решение задачи 2.1-40 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-41 Определить выход продукта R и степень превращения реагента А, если обратимая реакция А-2R протекает до равновесия, когда xA=0,75 xA, равн, а соотношение концентраций продукта и реагента СR: СА=1.
Скачать решение задачи 2.1-41 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-43 Окисление аммика воздухом до образования оксида азота как целевого продукта протекает по следующим реакциям:
4NH3+5O2=4NO+6H2O
4NH3+3O2=2N2+6H2O
4NH3+4O2=2N2O+6H2O
Селективность по NO равна 0,92, степень окисления аммиака 0,98. Определить сколько дополнтельно образуется азота, если на процесс поступает аммиачно-воздушная смесь в количестве 1000 м3 при концентрации аммиака 9% объемных долей.
Скачать решение задачи 2.1-43 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-45 Для параллельной жидкофазной реакции первого порядка определить интегральную селективность и выход по продукту R, если начальная концентрация реагента А равна 1,42 кмоль/м3, общая степень превращения 0,89, а концентрация продукта R = 0,438 кмоль/м3.
Скачать решение задачи 2.1-45 (В.И. Игнатенков, В.С Бесков) (цена 150р)
Задача 2.1-46 Для последовательной реакции A → R → S определить интегральную селективность по продукту R, выход этого продукта и общую степень превращения реагента А, если после окончания реакции в смеси концентрации веществ составили, кмоль/м3: CA = 0,2, CR = 0,56, CS = 0,24
Скачать решение задачи 2.1-46 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2-1-47 При проведении двух последовательных реакций первого порядка гидратации ацетилена и дегидратации ацетальдегида из 1 моль ацетилена и 10 моль водяного пара получено 0,4 моль ацетальдегида и 0,025 моль кротонового альдегида. Рассчитать общую и частные степени превращения ацетилена (по обеим реакциям), состав полученной реакционной смеси, интегральную селективность по ацетальдегиду и выход ацетальдегида.
C2H2 + H2O → CH3CHO
2CH3CHO → CH3-CH=CH-CHO
Скачать решение задачи 2.1-47 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2-1-48. При проведении последовательной реакции дегидрирования
C4H10 → C4H8 → C4H6
частные степени превращения бутана в бутилен и бутадиен составляют соответственно 0,38 и 0,04. Рассчитать состав полученной реакционной смеси, общую степень превращения бутана, интегральную селективность и выход по бутилену, если исходное количество бутана 21 моль.
Скачать решение задачи 2.1-48 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-49 Получение фенола состоит из трех стадий:
C6H6 + CH2CHCH3 → C6H5CH(CH3)2) →
→ C6H5C(CH3)2OOH → C6H5OH + CCH3)2O
Рассчитать расход бензола и пропан-пропиленовой фракции газов крекинга (30% об. долей пропилена и 70% объемных долей пропана) для производства 1 т фенола, если выход изопропилбензола из бензола составляет 90%, фенола из изопропилбензола через стадию окисления изопропилбензола в гидропероксид -93%. Молекулярная масса бензола -78, пропилена - 42, пропана – 44, фенола-94.
Скачать решение задачи 2.1-49 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-50. Определить расход аммиака и воздуха на 1 т моногидрата HNO3, если степень окисления NH3 в NO равна 0,96, а степень абсорбции оксидов азота - 0,98. Расход воздуха учитывать только в реакциях окисления NH3 и NO.
Брутто-реакция: NH3 + 2O2 = HNO3 + H2O
Молекулярная масса: NH3 - 17; HNO3 - 63.
Скачать решение задачи 2.1-50 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-51. Рассчитать расход аммиака и воздуха на 1 т 50% азотной кислоты при степени окисления аммиака в оксид азота 0,95 и степени абсорбции оксидов азота 0,96. при расчете расхода воздуха учитывать только стехиометрию реакций по схеме NH3 -> NO -> NO2 -> HNO3
Скачать решение задачи 2.1-51 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-52 Рассчитать количество и состав газа, получаемого при окислении аммиачно-воздушной смеси, содержащей 6% массовых долей аммиака в воздухе. Степень окисления аммиака равна 0,97, выход оксида азота равен 95%. Считать, что аммиак окисляется до оксида азота и азота.
Скачать решение задачи 2.1-52 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-53 Нагрузка на реактор синтеза аммиака составляет 2000 м3/ч азотоводородной смеси стехиометрического состава, находящейся под давлением 2,5 МПа и температуре 700 К. Газ на выходе из реактора содержит 20 % объемных долей аммиака, тепловой эффект реакции - 112 кДж. Рассчитать состав газовой смеси на выходе из реактора и количество выделенной теплоты.
Скачать решение задачи 2.1-53 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-54 Определить количество аммиака, требуемое для производства 100 т/год 100 %-ной азотной кислоты, и расход воздуха на окисление аммиака, если цех работает 355 дней в году, выход оксида азота 0,97, степень абсорбции оксидов азота 0,92, содержание аммиака в сухой аммиачно-воздушной смеси 9,5 % объемных долей.
Скачать решение задачи 2.1-54 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-57 Конверсия метана водяным паром до оксида углерода и водорода сопровождается поглощением 206 кДж теплоты на стехиометрию реакции. В реактор поступает реакционная смесь в мольном соотношении пар/метан равном 3:1. Определить степени превращения метана и водяного пара, общее количество поглощенной теплоты при переработке 10 м3/с исходной смеси, если на выходе из реактора содержится 10 % объемных долей окиси углерода.
Скачать решение задачи 2.1-57 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-58 Определить количество теплоты, необходимое для получения водорода каталитической конверсией метана по реакции:
CH4 + H2O = CO + 3H2 - 206 кДж
Степень превращения метана равна 0,92, объемное отношение в исходной парогазовой смеси составляет 1:2,8. температура в зоне реакции -980 , температура поступающих в реактор реагентов - 130 . Потери теплоты в окружающую среду составляют 5% от поступающей. Расчет вести на 1000 м полученного водорода. Молярные теплоемкости газов, кДж/(кмоль град): СH4 = 36,8; H2O = 36; CO = 30,5; H2 = 29,5
Скачать решение задачи 2.1-58 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-59 Составить материальный баланс процесса паровой конверсии метана СН4 + Н20 = СО + ЗН2, если степень превращения СН4 равна 0,95, мольное отношение Н20/СН4 = 3. Расчет вести на 1000 и3 исходной парогазовой смеси.
Скачать решение задачи 2.1-59 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-60 Определить расход воздуха для дожигания 100м3 отходящих газов, состоящих, об.доли%:

Рассчитать состав газовой смеси после дожигания:
2CO + O2 = 2CO2
Скачать решение задачи 2.1-60 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-61 Определить расход сухого воздуха, количество и состав обжигового газа, количество и состав огарка при обжиге 1 т/ч флотационного колчедана, содержащего 38% массовых долей серы. В колчедане выгорает 96% серы. Коэффициент избытка воздуха составляет 1,4 по отношению к стехиометрии
FeS2 + 11O2 = 2Fe2O3 + 8SO3
Скачать решение задачи 2.1-61 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-62. Рассчитать выход и определить количество выделенной теплоты при обжиге 1000кг серного колчедана, содержащего 41% массовых долей серы при влажности 7,4%массовых долей. В огарке содержится 0,5%массовых долей серы. Реакция:
4FeS2 + 11O2 = 2Fe2O3 + 8SO2 + 3415 кДж.
Скачать решение задачи 2.1-62 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-63 Рассчитать количество теплоты, выделяемой при переработке 1000 сернистого газа, состоящего из 10% объемных долей SО2 в воздухе. Степень превращения SО2 равна 90%. Каким будем при этом состав смеси на выходе из реактора (в об долях,%)? Реакция:
SО2 +0,5О2 → SО3+ 92000Дж.
Составить материальный баланс реактора окисления SО2 в SО3
При переработке 10000 /ч сернистого газа, содержащего 10% объемных долей в воздухе SО2 .
Скачать решение задачи 2.1-63 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-64 Оксид этилена получают окислением этилена по реакциям:
С2H4 + 0,5O2 = C2H4O + 117кДж
C2H4 + 3O2 = 2CO2 + 2H2O + 1217кДж.
Рассчитать объемный расход исходной смеси (8% объемных долей этилена, 19,32% объемных долей кислорода, остальное-азот). для получения 250м /ч оксида этилена, если селективность по нему составляет 0,65, а степень превращения этилена равна 0,98. Определить также общее количество выделившейся при этом теплоты.
Скачать решение задачи 2.1-64 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-65. Рассчитать материальный баланс производства хлора методом электролиза водного раствора NaCl
2NaCl + 2H2O = 2NaOH + Cl2 + H2
Концентрация NaCl в растворе 310г/л. Плотность раствора при условиях электролиза 1,17кг/л. Степень разложения NaCl - 50%. Расчет вести на 1000м хлора.
Скачать решение задачи 2.1-65 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-66 Составить материальный и тепловой балансы сжигания сероводорода для сернокислотного завода производительностью 25 т/ч моногидрата (100% H2SO4). Исходный газ содержит, объемные доли, %: H2S - 91; Н2О - 6; N2 - 3. Средняя его теплоемкость 1,68 кДж/(м3*град). На 1 м3 сероводородного газа в печь подается 23 м3 воздуха (в пересчете на сухой). Содержание влаги в воздухе - 8% объемных долей. Температура поступающего воздуха и сероводородного газа 33 °С. Производственные потери 20% массовых долей. Потери теплоты в окружающую среду 5%. Теплота сгорания H2S -519,3 кДж/моль, теплоемкости, кДж/(м3*град): SO2 - 1,47; воздуха -1,34. Определить также температуру выходящих газов.
Скачать решение задачи 2.1-66 (В.И. Игнатенков, В.С Бесков) (цена 200р)
Задача 2.1-69 Пиролиз бутана протекает по реакциям:
C4H10 - C3H6 + CH4
C4H10 = C2H4 + C2H6
Рассчитать степень превращения бутана, если в конечно смеси его концентрация составляет 0,1 молярной доли.
Скачать решение задачи 2.1-69 (В.И. Игнатенков, В.С Бесков) (цена 200р)


