10 Решение задач по термодинамике (Семиохин) МГУ Ломоносова
Задача 1 (задачник Семиохин) Вычислить молекулярную массу озона, если при 28,2 °С в колбе объемом 235,67 см3 при давлении озона 274,4 мм рт. ст. находилось 0,1626 г озона.
Ответ: М = 47,25 г*моль-1.
Скачать решение задачи 1 (задачник Семиохин) (цена 50р)
Задача 2 (задачник Семиохин) Молекулярная масса диэтилового эфира определялась по методу Майера. Получены следующие данные: вес эфира 0,1023 г, объем вытесненного воздуха 35,33 см3, температура 32,5 °С, атмосферное давление 743,95 мм рт. ст. Вычислите молекулярную массу эфира.
Ответ: М = 74,19 г*моль-1.
Скачать решение задачи 2 (задачник Семиохин) (цена 50р)
Задача 3 (задачник Семиохин) Некоторый газ имел следующие плотности при 300 К
Давление, атм 0,400 0,800 1,000
Плотность, г*л-1 1,512 3,038 3,900
Определите молекулярную массу газа с точностью, которую могут дать эти данные.
Ответ: М = 91,03 г*моль-1.
Скачать решение задачи 3 (задачник Семиохин) (цена 50р)
Задача 4 (задачник Семиохин) Зависимость плотности метиламина от давления исследовалась при температуре 0 °С. Были получены следующие данные:
Давление, атм 0,200 0,500 0,800
Плотность, г*л-1 0,2796 0,7083 1,1476
Определите молекулярную массу этого соединения.
Ответ: М = 31,07 г*моль-1.
Скачать решение задачи 4 (задачник Семиохин) (цена 50р)
Задача 5 (задачник Семиохин) Вычислите давление, создаваемое 2 молями хлорбензола, занимающими объем 10 л при 25 °С. Используйте: а) закон идеального газа; б) уравнение Ван-дер-Ваальса (а = 25,43 л2*атм*моль-2, b = 0,1453 л*моль-1).
Ответ: а) р = 4,90 атм; б) р = 4,02 атм.
Скачать решение задачи 5 (задачник Семиохин) (цена 50р)
Задача 6 (задачник Семиохин) Коэффициент сжимаемости z = pV/RT для СО2 при 0 °С и 100 атм равен 0,2007. Вычислите объем 0,1 моля газа при этих условиях. Используйте: а) закон идеального газа; б) коэффициент сжимаемости.
Ответ: а) V1= 22,4*10-3 л; б) V2= 4,5*10-3 л.
Скачать решение задачи 6 (задачник Семиохин) (цена 50р)
Задача 7 (задачник Семиохин) Коэффициент сжимаемости z = pV/RT для азота при –50 °С и 800 атм равен 1,95; при 100 °С и 200 атм – 1,10. Объем некоторого количества азота при –50 °С и 800 атм равен 1 л. Вычислите объем того же количества азота при 100 °С и 200 атм.
Ответ: V2= 3,77 л.
Скачать решение задачи 7 (задачник Семиохин) (цена 50р)
Задача 8 (задачник Семиохин) Зависимость коэффициента термического расширения гелия a [a=1/V(dV/dT)p] от давления приведена ниже:
р, мм рт. ст. 504,8 520,5 760,1 1102,9 1116,5
a*106 3658,9 3660,3 3659,1 3658,2 3658,1
Вычислите температуру (°С), соответствующую абсолютному нулю.
Ответ: t0= -273,16 °С.
Скачать решение задачи 8 (задачник Семиохин) (цена 50р)
Задача 9 (задачник Семиохин) Плотность (г*л-1) некоторого газа при 300 К определяется уравнением: а = 2,000 р + 0,1200 р2, где р – давление в атмосферах. Вычислите молекулярную массу газа с точностью до четырех значащих цифр.
Ответ: М = 49,23 г*моль-1.
Скачать решение задачи 9 (задачник Семиохин) (цена 50р)
Задача 10 (задачник Семиохин) Смесь гелия и аргона весит 5 г и занимает объем 10 л при 25 °С и 1 атм. Определите состав смеси в массовых процентах.
Ответ: gHe= 25,2 %; gAr= 74,8 %.
Скачать решение задачи 10 (задачник Семиохин) (цена 50р)
Задача 11 (задачник Семиохин) Вычислите плотность воздуха, насыщенного водяным паром при 25 °С. Давление пара воды при этой температуре равно 23,7 мм рт. ст. Состав сухого, свободного от СО2 воздуха: 78,1 об % N2, 21 об % О2 и 0,9 об % Ar. Общее давление равно 1 атм.
Ответ: 1,169 г*л-1.
Скачать решение задачи 11 (задачник Семиохин) (цена 50р)
Задача 12 (задачник Семиохин) Покажите, что при низких плотностях уравнение Ван-дер-Ваальса для 1 моля: (p + a/V2)*(V-b) = RT и уравнение Дитеричи: p(V – b) = RTea/RTV дают по существу одинаковый результат для давления р.
Примечание: в уравнении Дитеричи разложите экспоненту в ряд
ex = 1 + x + x2/2! + ….
Ответ: p = RT/(V-b) – a/V2
Скачать решение задачи 12 (задачник Семиохин) (цена 50р)
Задача 13 (задачник Семиохин) Некоторый газ подчиняется уравнению состояния: p = RT/(V-bT) – a/V3 , где V - мольный объем, а и b – характеристические постоянные газа. Покажите, что a = 4RTkpVkp/3 и b = Vkp/2Tkp, где Tkp и Vkp – критические величины.
Скачать решение задачи 13 (задачник Семиохин) (цена 50р)
Задача 14 (задачник Семиохин) Каждый из двух сферических сосудов (объём каждого сосуда 22,4 л) заполнили одним молем азота при температуре 25 °С и давлении 1 атм. Затем сосуды соединили тонкой пустой трубкой незначительного объема. Один шар поместили в термостат при температуре 100 °С, а другой – при 0 °С. Определите конечное давление в системе и число молей азота в каждом шаре.
Ответ: р1 = р2 = 1,16 атм; n1 = 0,846 моля, n2 = 1, 154 моля.
Скачать решение задачи 14 (задачник Семиохин) (цена 50р)
Задача 15 (задачник Семиохин) Покажите, что для газа Ван-дер-Ваальса Tkp = 8a/27bR, Vкр = 3nb и pкр = a/27b2, где Tkp, Vkp и Pkp – критические величины газа. Уравнение Ван-дер-Ваальса для n молей газа имеет вид: (p+n^2*a/V2)(V-nb) = nRT
Скачать решение задачи 15 (задачник Семиохин) (цена 50р)
Задача 2-1 (задачник Семиохин) а) Определите, каким процессам соответствуют следующие стадии для одного моля идеального одноатомного газа, проведенного через
обратимый цикл и значения р в атм в точках 1, 2 и 3.
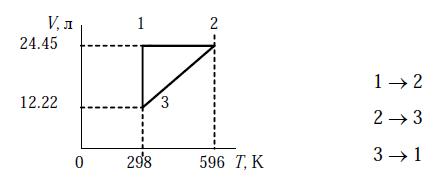
Ответ: P1 = 1, P2 = 2, P3 = 2 атм.
б) Вычислите следующие величины (Дж?моль-1) в таблице, используя данные задачи а):
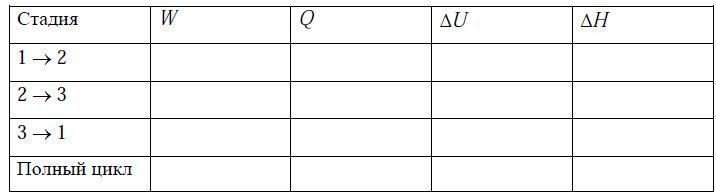
Скачать решение задачи 2-1 (задачник Семиохин) (цена 50р)
Задача 2-2 (задачник Семиохин) а) Определите, каким процессам соответствуют следующие стадии для одного моля идеального одноатомного газа, проведенного через обратимый цикл и значения V в л. в точках 1, 2, 3.
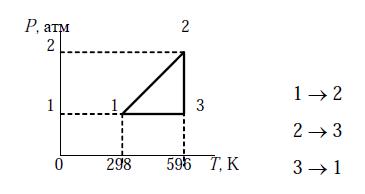
Ответ: V1 = V2 = 24,45 л; V3 = 48,90 л.
б) Вычислите следующие величины (в Дж*моль-1) в таблице, используя
данные первой части задачи:
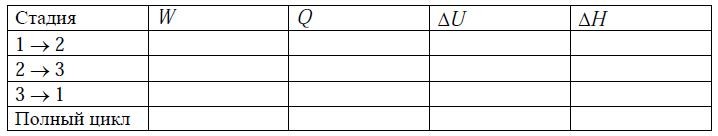
Скачать решение задачи 2-2 (задачник Семиохин) (цена 50р)
Задача 2-10 (задачник Семиохин) Покажите, что коэффициент Джоуля – Томсона mJT = (dT/dp)H может быть представлен в виде двух выражений:
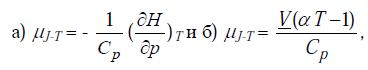
где a - коэффициент расширения газа, равный a=1/V(dV/dT)p
Скачать решение задачи 2-10 (задачник Семиохин) (цена 50р)


